Altern ist kein Zufall, sondern ein biologischer Prozess, der auf Zellebene beginnt. Telomere verkürzen sich, Mitochondrien verlieren ihre Effizienz, und DNA-Schäden häufen sich über Jahrzehnte an. Wer versteht, was in unseren Zellen passiert, kann gezielt gegensteuern und die eigene Gesundheitsspanne verlängern.
Key Takeaways 🔬
- Telomere sind die biologischen „Schutzkappen“ der Chromosomen und verkürzen sich bei jeder Zellteilung.
- Seneszente Zellen (sogenannte „Zombie-Zellen“) hören auf, sich zu teilen, schädigen aber umliegendes Gewebe durch Entzündungssignale.
- Mitochondriale Dysfunktion ist eine der zentralen Ursachen für Energieverlust im Alter.
- Epigenetische Veränderungen bestimmen, wie aktiv oder inaktiv unsere Gene im Laufe des Lebens sind.
- Oxidativer Stress beschleunigt Zellschäden, ist aber durch Ernährung und Bewegung teilweise beeinflussbar.
- Die sogenannten Hallmarks of Aging (Lopez-Otin et al., 2013) beschreiben neun molekulare Mechanismen des Alterns.
- Lebensstilfaktoren wie Schlaf, Sport und Ernährung haben nachweisbaren Einfluss auf die biologische Alterungsrate.
- Neue Forschungsfelder wie Senolytika und epigenetische Reprogrammierung zeigen vielversprechende Ansätze.
Was bedeutet Altern auf zellulärer Ebene?
Altern auf Zellebene bedeutet, dass sich Reparaturmechanismen verschlechtern, Schäden akkumulieren und Zellen ihre Funktion verlieren. Das ist kein einzelner Prozess, sondern ein Zusammenspiel vieler molekularer Vorgänge, die sich gegenseitig verstärken.
Die Wissenschaft des Alterns beschäftigt sich seit Jahrzehnten mit diesen Mechanismen. Ein Meilenstein war die Veröffentlichung der „Hallmarks of Aging“ durch Lopez-Otin und Kollegen im Jahr 2013 im Fachjournal Cell. Sie definierten neun zentrale Merkmale des zellulären Alterns, darunter:
- Genomische Instabilität
- Telomerverkürzung
- Epigenetische Veränderungen
- Verlust der Proteostase (Proteinfaltung und -abbau)
- Deregulierte Nährstoffsensorik
- Mitochondriale Dysfunktion
- Zelluläre Seneszenz
- Stammzellerschöpfung
- Veränderte interzelluläre Kommunikation
Merke: Kein einzelner Mechanismus ist allein verantwortlich. Es ist das Zusammenspiel dieser Prozesse, das uns altern lässt.
Wie funktionieren Telomere, und warum verkürzen sie sich?
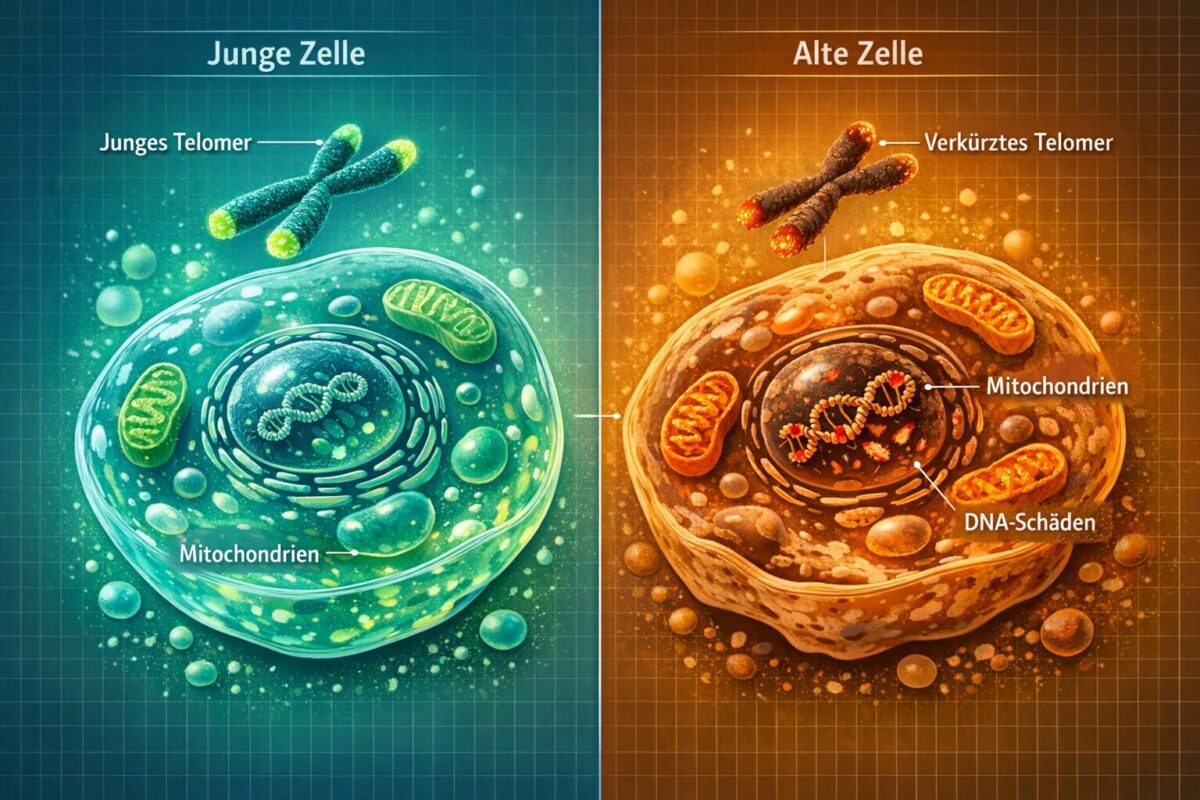
Telomere sind schützende DNA-Sequenzen am Ende jedes Chromosoms. Bei jeder Zellteilung werden sie ein kleines Stück kürzer. Unterschreiten sie eine kritische Länge, kann die Zelle sich nicht mehr teilen und wird entweder abgebaut oder seneszent.
So funktioniert der Prozess Schritt für Schritt:
- Eine Körperzelle teilt sich, um Gewebe zu erneuern.
- Das Enzym DNA-Polymerase kann das Ende des Chromosoms nicht vollständig kopieren.
- Die Telomere verlieren bei jeder Teilung etwa 50–200 Basenpaare (Schätzung basierend auf Laborstudien, Blackburn et al., 2009).
- Nach etwa 50–70 Teilungen (Hayflick-Limit) stoppt die Zelle ihre Teilung.
- Kurze Telomere aktivieren Stresssignale, die Entzündungen fördern.
Das Enzym Telomerase kann Telomere verlängern, ist in den meisten Körperzellen aber kaum aktiv. Stammzellen und Keimzellen bilden eine Ausnahme. Krebszellen nutzen Telomerase ebenfalls, was ihre unkontrollierte Teilung ermöglicht.
Wähle diesen Ansatz, wenn… du verstehen willst, warum chronischer Stress das biologische Alter beschleunigt: Stress erhöht Cortisol, was nachweislich mit schnellerer Telomerverkürzung assoziiert ist (Epel et al., 2004, PNAS).
Was sind seneszente Zellen, und warum sind sie gefährlich?
Seneszente Zellen sind Zellen, die aufgehört haben, sich zu teilen, aber nicht absterben. Sie senden stattdessen entzündungsfördernde Signale aus, den sogenannten SASP (Senescence-Associated Secretory Phenotype).
Diese „Zombie-Zellen“ sind problematisch, weil sie:
- Chronische Entzündungen im umliegenden Gewebe auslösen
- Gesunde Nachbarzellen zur Seneszenz verleiten können
- Mit altersbedingten Erkrankungen wie Arthritis, Arteriosklerose und Typ-2-Diabetes assoziiert sind
Forschungsgruppen arbeiten an Senolytika, also Wirkstoffen, die seneszente Zellen gezielt beseitigen. Substanzen wie Dasatinib und Quercetin zeigen in Tiermodellen positive Effekte (Kirkland & Tchkonia, 2017, Journal of Internal Medicine). Beim Menschen ist die Forschung noch im frühen Stadium.
Häufiger Denkfehler: Seneszente Zellen sind nicht nur schädlich. In der Wundheilung und während der Embryonalentwicklung spielen sie eine wichtige, kurzfristig nützliche Rolle. Erst ihre dauerhafte Ansammlung im Alter wird zum Problem.
Welche Rolle spielen Mitochondrien beim Altern?
Mitochondrien sind die Energiefabriken der Zelle. Im Alter verlieren sie Effizienz, produzieren mehr freie Radikale und reparieren sich schlechter. Das führt zu weniger ATP (Zellenergie) und mehr oxidativem Stress.
Mitochondriale Dysfunktion äußert sich durch:
| Symptom | Zelluläre Ursache |
|---|---|
| Müdigkeit und Leistungsabfall | Weniger ATP-Produktion |
| Muskelabbau | Schlechtere Energieversorgung der Muskelzellen |
| Kognitive Verlangsamung | Neuronen mit hohem Energiebedarf leiden früh |
| Erhöhte Entzündungsmarker | Freigesetzte mitochondriale DNA aktiviert Immunzellen |
Die gute Nachricht: Ausdauertraining stimuliert die Mitochondrienbiogenese, also die Neubildung von Mitochondrien. Der Signalweg läuft über PGC-1α, einen zentralen Regulator des Energiestoffwechsels. Regelmäßige körperliche Aktivität ist damit eine der wirksamsten bekannten Maßnahmen gegen mitochondriale Alterung.
Wer sich für ganzheitliche Ansätze interessiert, findet im Gesundheitsbereich weitere Artikel zu Körper, Geist und natürlichen Heilmethoden.
Was sind epigenetische Veränderungen, und wie beeinflussen sie das Altern?
Epigenetische Veränderungen sind Modifikationen, die nicht die DNA-Sequenz selbst verändern, aber bestimmen, welche Gene aktiv oder inaktiv sind. Im Alter verschieben sich diese Muster systematisch.
Die Wissenschaft des Alterns nutzt epigenetische Uhren als Messinstrument. Der bekannteste Ansatz ist die Horvath-Uhr (Horvath, 2013, Genome Biology), die auf DNA-Methylierungsmustern basiert und das biologische Alter einer Person bestimmen kann, unabhängig vom kalendarischen Alter.
Was beeinflusst epigenetische Muster?
- 🥗 Ernährung: Methyl-Gruppen-Spender wie Folat, B12 und Cholin unterstützen gesunde Methylierungsmuster.
- 🏃 Bewegung: Sport verändert Histonmodifikationen und DNA-Methylierung in Muskel- und Gehirnzellen.
- 😴 Schlaf: Schlafmangel beschleunigt epigenetische Alterung nachweislich.
- 🚬 Rauchen: Einer der stärksten bekannten Beschleuniger epigenetischer Alterung.
- 🧘 Stress: Chronischer Stress verändert Methylierungsmuster in stressrelevanten Genen.
Wichtig: Epigenetische Veränderungen sind zum Teil reversibel. Das macht sie zu einem attraktiven Ziel für Anti-Aging-Interventionen.
Wie beschleunigt oxidativer Stress das zelluläre Altern?
Oxidativer Stress entsteht, wenn freie Radikale (reaktive Sauerstoffspezies, ROS) die körpereigenen Abwehrmechanismen überlasten. ROS entstehen als Nebenprodukt des normalen Stoffwechsels, aber auch durch externe Faktoren wie UV-Strahlung, Umweltgifte und schlechte Ernährung.
Folgen von oxidativem Stress auf Zellebene:
- DNA-Strangbrüche und Mutationen
- Schäden an Proteinen und Lipiden in Zellmembranen
- Mitochondriale Dysfunktion (ein Teufelskreis: geschädigte Mitochondrien produzieren mehr ROS)
- Aktivierung von Entzündungswegen
Der Körper besitzt eigene Antioxidationssysteme, darunter Superoxiddismutase (SOD), Katalase und Glutathion. Diese Systeme werden im Alter weniger effizient.
Praktische Konsequenz: Eine antioxidantienreiche Ernährung mit viel Gemüse, Beeren und Olivenöl unterstützt diese Systeme. Hochdosierte Antioxidantien-Supplemente hingegen zeigen in klinischen Studien kein einheitlich positives Bild und können in manchen Fällen kontraproduktiv sein.
Wer sich für natürliche Heilmittel interessiert, kann auch einen Blick auf Pflanzenheilkunde werfen, wo traditionelle Pflanzenanwendungen beschrieben werden.
Welche Lebensstilfaktoren verlangsamen das zelluläre Altern nachweislich?
Die Wissenschaft des Alterns zeigt klar: Lebensstil beeinflusst die biologische Alterungsrate messbar. Das ist keine Spekulation, sondern durch Biomarker wie Telomerlänge, epigenetische Uhren und Entzündungsmarker belegbar.
Evidenzbasierte Maßnahmen im Überblick:
| Maßnahme | Mechanismus | Evidenzgrad |
|---|---|---|
| Ausdauertraining (150 min/Woche) | Mitochondrienbiogenese, Telomerschutz | Hoch |
| Kalorienrestriktion / Intervallfasten | mTOR-Hemmung, Autophagie-Aktivierung | Mittel-Hoch |
| Ausreichend Schlaf (7–9 Stunden) | DNA-Reparatur, Hormonregulation | Hoch |
| Mediterrane Ernährung | Entzündungshemmung, epigenetischer Schutz | Hoch |
| Stressreduktion (Meditation, Natur) | Cortisol-Senkung, Telomerschutz | Mittel |
| Nikotinverzicht | Epigenetische Stabilisierung | Sehr Hoch |
| Soziale Verbundenheit | Neuroendokrine Regulierung | Mittel |
Wähle Intervallfasten, wenn… du eine Methode suchst, die Autophagie aktiviert, also den zellulären Selbstreinigungsprozess, bei dem beschädigte Zellbestandteile abgebaut werden. Dieser Prozess nimmt im Alter ab und kann durch Fastenphasen reaktiviert werden.
Manche Menschen verbinden körperliche Gesundheitspraktiken mit ganzheitlichen Ansätzen. Heilsteine wie Hämatit oder Amethyst werden traditionell mit Erdung und Entspannung assoziiert und können als ergänzende Rituale zur Stressreduktion dienen, auch wenn ihre Wirkung wissenschaftlich nicht belegt ist.
Was sagt die aktuelle Forschung 2026 zu Anti-Aging-Interventionen?
Die Forschung zur Wissenschaft des Alterns bewegt sich 2026 in mehrere Richtungen gleichzeitig. Einige Ansätze sind bereits in klinischen Studien, andere noch in frühen Phasen.
Vielversprechende Forschungsfelder:
- Senolytika: Wirkstoffe wie Quercetin und Fisetin, die seneszente Zellen beseitigen, befinden sich in Phase-II-Studien beim Menschen.
- NAD+-Vorläufer: NMN (Nicotinamidmononukleotid) und NR (Nicotinamidribosid) sollen den NAD+-Spiegel erhöhen, der im Alter sinkt. Tiermodelle zeigen positive Effekte; humane Langzeitdaten fehlen noch weitgehend.
- Rapamycin: Ein mTOR-Hemmer, der in Tiermodellen die Lebensspanne verlängert. Klinische Studien beim gesunden Menschen laufen.
- Epigenetische Reprogrammierung: Yamanaka-Faktoren können Zellen in einen jüngeren Zustand versetzen. Dieser Ansatz ist noch experimentell, gilt aber als einer der spannendsten.
- GLP-1-Agonisten: Ursprünglich für Diabetes entwickelt, zeigen sie in neuen Studien mögliche Effekte auf Entzündung und metabolisches Altern.
Wichtiger Hinweis: Kein Supplement und keine Intervention hat bisher in kontrollierten Humanstudien bewiesen, dass sie die maximale menschliche Lebensspanne verlängert. Wer Supplemente erwägt, sollte dies mit einem Arzt besprechen.
Wer seinen persönlichen Biorhythmus besser verstehen möchte, kann den Biorhythmus-Rechner nutzen, um körperliche, emotionale und intellektuelle Zyklen zu beobachten.
FAQ: Die Wissenschaft des Alterns – Was in unseren Zellen passiert
Was sind die wichtigsten Ursachen des zellulären Alterns?
Die Hauptursachen sind Telomerverkürzung, DNA-Schäden, mitochondriale Dysfunktion, zelluläre Seneszenz und epigenetische Veränderungen. Diese Prozesse wirken zusammen und verstärken sich gegenseitig.
Kann man das biologische Alter messen?
Ja. Epigenetische Uhren wie die Horvath-Uhr messen DNA-Methylierungsmuster und können das biologische Alter bestimmen. Kommerzielle Tests sind verfügbar, aber ihre klinische Aussagekraft ist noch begrenzt.
Ist Altern genetisch vorbestimmt?
Genetik spielt eine Rolle, aber Studien an eineiigen Zwillingen zeigen, dass Lebensstil und Umwelt mindestens 50–70 Prozent der biologischen Alterungsrate erklären (Schätzung basierend auf Zwillingsstudien, Fraga et al., 2005).
Was ist der Unterschied zwischen Lebensspanne und Gesundheitsspanne?
Lebensspanne ist die Gesamtdauer des Lebens. Gesundheitsspanne bezeichnet die Jahre, in denen man frei von chronischen Erkrankungen und funktionell fit ist. Das Ziel moderner Longevity-Forschung ist, die Gesundheitsspanne zu maximieren.
Hilft Sport wirklich gegen Zellalterung?
Ja, nachweislich. Ausdauertraining fördert die Mitochondrienbiogenese, schützt Telomere und aktiviert Autophagie. Krafttraining erhält Muskelmasse und verbessert die metabolische Gesundheit, beides wichtige Faktoren für gesundes Altern.
Was ist Autophagie, und wie aktiviert man sie?
Autophagie ist der zelluläre Selbstreinigungsprozess, bei dem beschädigte Zellbestandteile abgebaut werden. Sie wird durch Fastenphasen (ab ca. 16 Stunden), Sport und Kalorienrestriktion aktiviert.
Sind Anti-Aging-Supplemente sinnvoll?
Manche zeigen in Studien Potenzial (z.B. NMN, Quercetin), aber belastbare Langzeitdaten beim Menschen fehlen. Grundlegende Maßnahmen wie Schlaf, Bewegung und Ernährung haben deutlich mehr Evidenz.
Was sind die Hallmarks of Aging?
Das sind neun molekulare Merkmale des Alterns, die 2013 von Lopez-Otin et al. in Cell beschrieben wurden. Sie umfassen u.a. genomische Instabilität, Telomerverkürzung und zelluläre Seneszenz.
Kann Stress das Altern beschleunigen?
Ja. Chronischer Stress erhöht Cortisol, was mit schnellerer Telomerverkürzung und epigenetischer Alterung assoziiert ist. Stressmanagement ist daher eine direkte Anti-Aging-Maßnahme.
Was bedeutet „biologisches Alter“ im Vergleich zum kalendarischen Alter?
Das kalendarische Alter ist die Zeit seit der Geburt. Das biologische Alter beschreibt den tatsächlichen Zustand der Zellen und Organe. Man kann 50 Jahre alt sein, aber biologisch wie 40 oder wie 60 altern, je nach Lebensstil und Genetik.
Fazit: Was du jetzt tun kannst
Die Wissenschaft des Alterns zeigt eindeutig: Altern ist kein passiver Prozess, dem man hilflos ausgeliefert ist. Auf Zellebene laufen spezifische, gut verstandene Mechanismen ab, und viele davon sind durch Lebensstilentscheidungen beeinflussbar.
Deine konkreten nächsten Schritte:
- Bewegung priorisieren: Mindestens 150 Minuten moderates Ausdauertraining pro Woche, ergänzt durch Krafttraining zweimal wöchentlich.
- Schlaf schützen: 7–9 Stunden pro Nacht sind keine Luxus, sondern biologische Notwendigkeit für DNA-Reparatur und Hormonregulation.
- Entzündungsarme Ernährung: Mediterrane Kost, reich an Gemüse, Olivenöl, Fisch und Hülsenfrüchten, unterstützt nachweislich mehrere Anti-Aging-Mechanismen gleichzeitig.
- Stress aktiv reduzieren: Meditation, Naturaufenthalte und soziale Verbundenheit haben messbare Effekte auf Cortisol und Telomerlänge.
- Rauchen aufgeben: Kein anderer Einzelfaktor beschleunigt epigenetisches Altern so stark wie Nikotin.
- Biologisches Alter beobachten: Epigenetische Tests können Motivation liefern, sind aber kein Ersatz für ärztliche Beratung.
Wer tiefer in ganzheitliche Gesundheitsthemen einsteigen möchte, findet im Magazin weitere inspirierende Artikel zu Körper, Natur und Wohlbefinden. Und wer neugierig auf spirituelle Werkzeuge zur Selbstreflexion ist, kann die spirituellen Rechner erkunden, von der Lebenszahl bis zum Biorhythmus.
Das Verständnis der Wissenschaft des Alterns ist der erste Schritt. Der zweite ist, täglich kleine, konsistente Entscheidungen zu treffen, die auf Zellebene einen Unterschied machen.
Quellen
- Lopez-Otin, C. et al. (2013). The Hallmarks of Aging. Cell, 153(6), 1194–1217. https://doi.org/10.1016/j.cell.2013.05.039
- Blackburn, E.H. et al. (2009). Human Telomere Biology: A Contributory and Interactive Factor in Aging, Disease Risks, and Protection. Science, 350(6265). https://doi.org/10.1126/science.aab3389
- Epel, E.S. et al. (2004). Accelerated telomere shortening in response to life stress. PNAS, 101(49), 17312–17315. https://doi.org/10.1073/pnas.0407162101
- Horvath, S. (2013). DNA methylation age of human tissues and cell types. Genome Biology, 14(10), R115. https://doi.org/10.1186/gb-2013-14-10-r115
- Fraga, M.F. et al. (2005). Epigenetic differences arise during the lifetime of monozygotic twins. PNAS, 102(30), 10604–10609. https://doi.org/10.1073/pnas.0500398102
- Kirkland, J.L. & Tchkonia, T. (2017). Cellular Senescence: A Translational Perspective. EBioMedicine, 21, 21–28. https://doi.org/10.1016/j.ebiom.2017.04.013
